1. 引言
随着国内能源需求日益增大和优质煤炭资源的大量减少,低阶煤逐渐成为炙手可热的煤炭资源。据统计,低阶煤在我国煤炭储量及产量中占很高比例,占全国已探明煤炭储量的55%以上 [1] 。低阶煤是处于低变质阶段的煤,水分、氧含量和挥发分较高,热值低,热稳定性差,直接开发利用较为困难 [2] 。为了避免导致高价值的化学能转化为低品位的热能,热解技术是低阶煤综合利用较好的途径 [3] 。通过干馏的方式,实现原煤的多级转化,是新型的低碳环保技术 [4] 。在煤热解过程中添加合适的催化剂可促进低阶煤的热解反应,提高热解转化率,因此低阶煤催化热解具有重要研究意义 [5] 。
近年来,一些研究人员研究了催化剂对煤热解反应的影响,以提高热解产物产率为目标,实现煤热解产物的定向转化 [6] [7] [8] 。而铁基催化剂价格低廉,对环境无污染,已成为最常用的催化剂之一。钟梅等 [9] 用Fe3+的硝酸盐处理脱灰和丰煤样,在热重分析仪中考察了处理煤样的失重特征和气体逸出规律,结果表明处理煤样的总失重率减少,CO2和H2的产量较原煤的高。Yu Fu等 [10] 以KCl、CaO和Fe2O3为催化剂,研究了黄陵煤的热解行为,通过气体组成的变化和动力学分析,讨论了催化机理,总结了催化剂对煤热解反应活性的影响。阎鑫等 [11] 采用低温溶液蒸发法制备NaFeS2纳米材料,研究了NaFeS2纳米材料在煤加氢热解工艺中的催化性能。Lei Zhang等 [12] 研究出Fe/γ-Al2O3催化剂在煤浆热解制氢反应中具有较好的催化活性,H2产率较高。
本研究采用水热合成法制备纳米级氧化铁催化剂,对其结构和形貌进行表征,并考察其在煤热解工艺中的催化性能。采用热重法研究海拉尔褐煤最有效的催化热解条件,建立热解过程的动力学模型,计算活化能E和指前因子A等热解动力学参数,并在固定床反应器上对热解产物产率进行了研究分析。
2. 实验
2.1. 实验原料
2.1.1. 煤样的制备
实验选用内蒙古海拉尔褐煤(HLE),经研磨筛选后选取粒径为200目以下的煤样,放入真空干燥箱中在80℃下干燥6 h,放入干燥器中备用。煤样的元素分析及工业分析见表1。

Table 1. Proximate and ultimate analyses of coal sample
表1. 煤样工业分析和元素分析
注:M为水分;A为挥发分;Fc为固定碳;V为挥发分。
2.1.2. 催化剂的制备
本实验采用水热合成法制备α-Fe2O3纳米立方体催化剂。称取FeC13∙6H2O和乌洛托品,将FeC13∙6H2O溶于10 ml二次去离子水中,将乌洛托品溶于30 m1去离子水中,并滴加盐酸调节pH值,使得pH = 1.8;边搅拌边将三氯化铁溶液缓慢滴加到含盐酸的乌洛托品溶液中,补加10 ml水,超声20 min后,将混合溶液倒入含有聚四氟乙烯内衬的不锈钢高压反应釜中,将反应釜放入预先加热到130℃的烘箱中,保温20 h。将高压釜中的产物全部倒入到离心机的PE离心管中,在3000 r/min高速下离心10 min;取出后,滤出上层溶液,重新加入适量的二次去离子水,并将其放入超声波清洗器中进行超声震荡,使沉淀的产物重新悬浮,再次进行离心;重复进行3次,将清洗过的产物转移至坩埚中,并放入到温度为65℃的烘箱中进行烘干,保温12 h。
2.2. 煤热解实验
煤热解实验在固定床反应装置上进行,实验装置流程示意图如图1所示,装置主要由配气系统、气体流量控制系统、预热器、管式反应器以及气体采集系统组成。
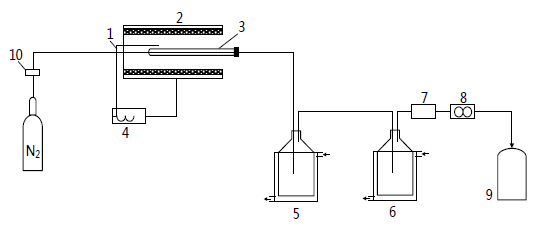 Schematic of coal pyrolysis setup. 1: thermocouple; 2: tube furnace; 3: quartz tube; 4: temperature controller; 5, 6: secondary condensing unit; 7: dryer; 8: gas flowmeter; 9: gas bag; 10: mass flow controller
Schematic of coal pyrolysis setup. 1: thermocouple; 2: tube furnace; 3: quartz tube; 4: temperature controller; 5, 6: secondary condensing unit; 7: dryer; 8: gas flowmeter; 9: gas bag; 10: mass flow controller
Figure 1. The yield of pyrolysis char
图1. 热解装置流程示意图。1:热电偶;2:管式炉;3:石英管;4:温度控制器;5,6:二级冷凝装置;7:干燥装置;8:气体流量计;9:集气袋;10:质量流量控制器
实验中使用高纯N2 (99.999%)为载气,流量为100 ml∙min−1。实验时,将煤粉和纳米α-Fe2O3催化剂以一定比例(1%、2%、3%、5%、10%)进行机械混合,将混合样品放入热解炉内,通入氮气20 min后再进行热解实验。热解实验采用程序升温的加热方式,管式炉升温速率为5℃/min,待温度自室温上升至110℃后,保温20 min,以脱除煤样中的自由水,再升至热解终温(450℃、500℃、550℃、600℃、650℃)后保温30 min,停止加热。从200℃开始收集气体,待开始降温后采气结束。将收集的气相产物用方正GC-4200型气相色谱仪对(H2、CO2、CH4、CO)进行气相色谱分析;热解产生的焦油在冷阱中冷却,冷却介质为冰水,温度在0℃~4℃之间;待温度降至室温时,将热解后的半焦取出称量,计算半焦收率。
2.3. 热重分析实验
本实验热重分析是在Setsys 16热分析仪上进行。实验过程中以惰性气体高纯氩气(99.999%)为保护气,载气流速为100 ml∙min−1。参与热重分析实验的样品质量约l0 mg,测定的温度区间为室温~1000℃,升温速率为10℃/min.
3. 结果与讨论
3.1. 催化剂的表征
用德国布鲁克D8-advance A25型X射线衍射仪分析了α-Fe2O3纳米催化剂的组成和结构,如图2所示,由X射线衍射图谱可看出α-Fe2O3衍射峰尖锐,说明结晶性较好,未检测到其他杂质峰的存在;用HT770003040701型透射电子显微镜观察样品的微观形貌,如图3所示,可观察到所制得样品为平行六面体的纳米颗粒。
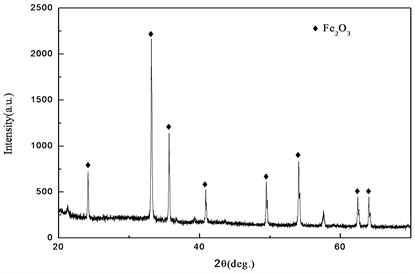
Figure 2. XRD pattern of the α-Fe2O3 catalyst
图2. α-Fe2O3催化剂X射线衍射图谱

Figure 3. SEM image of the α-Fe2O3 catalyst
图3. α-Fe2O3催化剂透射电子显微图
3.2. 热重分析
3.2.1. 不同催化剂添加量的热重分析
由图4及表2可知,加入Fe2O3的海拉尔褐煤热解效果比原煤的热解效果显著。在未加入Fe2O3纳米催化剂时,原煤的失重率是84.8%,加入添加剂Fe2O3后,海拉尔褐煤的热解转化率提高,最大失重率由原来的0.23上升到0.394,在催化剂加入5%时,失重率为79.7%,开始进行热解的温度由原煤的265.4℃降低到257.3℃,在温度到达580℃时,热解基本完成,说明催化剂加入有利于煤热解过程中挥发分的释放。但是当Fe2O3含量增加到10%时,煤样的失重率降低到75.2%,最大失重速率也是由0.394降低到0.19,这可能因为当催化剂过量时,会导致煤中孔隙结构的堵塞,进而影响热解过程的进行。考虑热解速率以及热解温度,催化剂的加入量为5%时,热解终温向低温段移动,失重率和热解速率达到最大,催化效果最好。

Figure 4. TG and DTG curves of different α-Fe2O3 addition (0%, 1%, 3%, 5%, 10%)
图4. α-Fe2O3的添加量为(0%、1%、3%、5%、10%)的TG和DTG曲线图

Table 2. The pyrolysis characteristic parameter of different α-Fe2O3 addition
表2. 不同α-Fe2O3的添加量热解特性参数表
3.2.2. 反应动力学分析
煤热解动力学是研究在热解过程中所涉及到的反应动力学参数,有利于描述煤热解所经历的复杂反应过程 [13] 。在动力学建模中,转化率x被定义为热解煤在时间t与初始煤的质量比如下:
(1)
w0、wt和
分别是样品的初始质量,t时刻样品的质量,反应结束时剩余样品的质量。
对煤催化热解的反应动力学模型建立过程如下:
(2)
根据Arrhenius经验方程可得
(3)
加热速率用β表示,
,β在热解过程中是固定值,将上式变形可得:
(4)
采用Coats-Redfern法 [14] 对式上式进行处理,得
当n = 1时,
(5)
当n ≠ 1时,
(6)
对一般的反应区和大部分的E而言,2RT/E远小于1,
可近似看做常数
。因此,当n = 1时,
对1/T作图;而当n ≠ 1时,
对1/T作图,都能得到一条直线,其斜率为
,即可求得活化能E和指前因子A。
加入催化剂后,海尔拉褐煤的热解过程被分为了两个一级反应的过程,由表3可以看出,第一阶段的活化能小于第二阶段的活化能,这是因为首先进行的是煤样的活泼热分解阶段,这一阶段煤中的侧链和官能团稳定性较差,容易分解,生成挥发分,化学键键能小,容易断裂分解,进而这阶段的活化能较小;第二阶段主要发生的是大分子的断裂,需要吸收了大量的热量,活化能增大。加入催化剂,使煤样分解的温度明显降低,随着添加量的增加,350℃~560℃范围内活化能先减小后增大,5%时活化能最低,与前面热重实验结果一致。
3.3. 热解产物产率分析
3.3.1. 液体产物
海拉尔褐煤以及添加5%的催化剂在不同温度条件下焦油产率分布如图5所示,可以看出在添加催化剂后,焦油产率明显增多,最高可达6.5%。随着温度的升高,热解产生焦油呈上升趋势,原煤热解的焦油由0.56%增至2.1%;添加催化剂热解后的焦油由1.1%增加到6.5%,但是在温度达到600℃后增加不明显,这与之前热重实验结果相符。在催化剂存在下热解聚焦油产率明显高于原煤热解后焦油的产率,说明纳米α-Fe2O3对原煤具有较强的催化解聚作用。

Table 3. The kinetic parameters of HLE coal in different reaction areas
表3. 海尔拉煤在各反应区域的动力学参数
3.3.2. 气相产物
如图6所示,图6(a)为不同终温下气相产率,随着温度的升高,原煤的气体产率不断增加,但在添加催化剂的情况下,产气率更高,最高为33.5%。图6(b)为热解终温600℃时,原煤和添加5%催化剂煤样热解气相组分的含量。由图可得,添加催化剂后各个组分的产量均有所提高。H2和CH4增加明显,分别增加了0.73和0.5。这主要因为过渡金属对氢化反应有较高的催化活性,可与煤中含氧官能团或不饱和烃中的化学键产生化学吸附,催化裂解烃类物质,使气体产物中H2和CH4含量大幅增加。
3.3.3. 固体产物
海拉尔褐煤以及在加入催化剂下的半焦产率变化过程如图7所示。在不添加催化剂的情况下,半焦的产率随着温度增加而下降。当加入添加剂后,半焦随温度的变化趋势与原煤类似。但是,半焦的产率明显减小,在600℃时,由原来的60%降到46%,减小了14%。
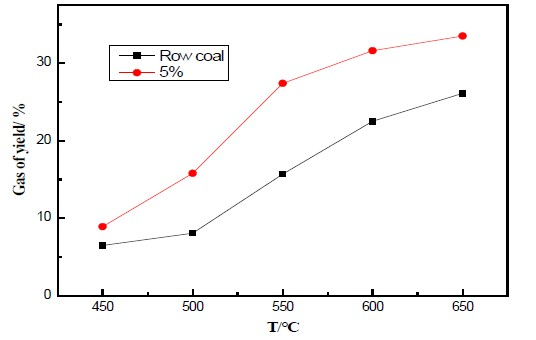 (a) 不同热解终温下气相产率
(a) 不同热解终温下气相产率  (b) 600℃时不同气体产率
(b) 600℃时不同气体产率
Figure 6. The yield of pyrolysis gas
图6. 热解气相产率
4. 结论
1) 通过热重实验对海拉尔褐煤失重过程进行研究,建立描述热解过程的动力学反应模型,并通过实验数据拟合动力学参数。热解动力学分析表明:在317℃~430℃和430℃~560℃两个区域温度区间内,褐煤的热解过程均符合一级单一反应模型,且不同添加量下催化热解的表观活化能均低于非催化热解的活化能。
2) 以提高热解煤气、焦油收率为目标进行催化热解实验,当纳米Fe2O3添加量为5%时,热解终温向低温移动,同时焦油产率由0.56%增加到6.5%,气相产率由6.89%增至33.5%,催化效果达到最佳。
基金项目
自治区高等学校科学技术研究项目(NGY2018-036);宁夏高等学校一流学科建设资助项目(NXYLXK2017A04);中国科学院西安分院“西部青年学者”B类项目(XAB2016AW03)。
NOTES
*通讯作者。